葡萄膜黑色素瘤是最常见的眼内肿瘤,在中国,其发病率则仅次于视网膜母细胞瘤,居眼内肿瘤的第二位。Immunocore是一家晚期生物技术公司,致力于开发新型T细胞受体(TCR)双特异性免疫疗法,Immunocore今日宣布,美国食品药品监督管理局(FDA)已授予tebentafusp(IMCgp100)“突破性疗法称号”(BTD),以治疗不可切除或转移性葡萄膜黑色素瘤(mUM)成年患者。
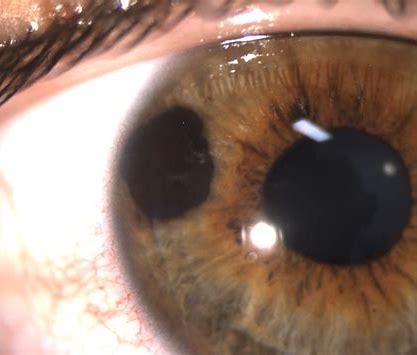


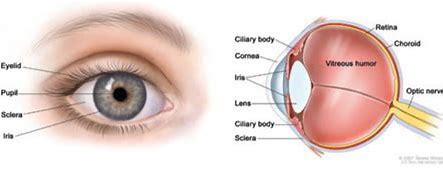 在对先前未经治疗的转移性葡萄膜黑色素瘤患者进行的一项随机III期临床试验(IMCgp100-202研究)中,中期分析表明,tebentafusp能够显著延长患者总生存率(OS),且优于其他免疫疗法,因此该试验达到了主要终点。
在对先前未经治疗的转移性葡萄膜黑色素瘤患者进行的一项随机III期临床试验(IMCgp100-202研究)中,中期分析表明,tebentafusp能够显著延长患者总生存率(OS),且优于其他免疫疗法,因此该试验达到了主要终点。
此前,Tebentafusp还获得了FDA的“快速通道资格”和“孤儿药称号”,以及英国早期药物计划下的“有前途的创新药物称号”。Immunocore将与FDA合作,以促进tebentafusp的上市。如果获得批准,Immunocore相信tebentafusp将是40年来治疗转移性葡萄膜黑色素瘤的一种新疗法。
Immunocore首席执行官Bahija Jallal表示:“我们很高兴FDA根据我们2020年11月宣布的III期临床试验的生存获益,授予替tebentafusp突破性疗法称号。患者迫切需要批准的治疗方法来治疗这种罕见且具有侵略性的黑色素瘤”。
原始出处:
https://www.firstwordpharma.com/node/1802311?tsid=4